Hvad er antibiotika?
Bakterier kan udvikle resistens mod antibiotika. Antibiotika er bakteriegift, og det findes naturligt i naturen hvor bakterier og svampe bruger det til kemisk krigsførelse. I 1928 opdagede Alexander Flemming at pinicillinsvampen lavede antibiotika som kunne bekæmpe bakterier. Det var en kæmpe opdagelse som har reddet millioner af menneskeliv fra bakterieinfektioner. Det fik han selvfølgelig en nobelpris for.

MRSA er multiresistente bakterier og spredes især fra grise i landbruget, og 84 % af de smittede i Danmark har fået smitten fra grise.
I dag findes der 9 hovedgrupper af antibiotika, hvor penicillin er den mest kendte, men desværre er de ved at miste deres effekt mod bakterier. Resistente mod antibiotika hos bakterier er ved at udvikle sig til en af de største trusler mod verdens befolkning.

På hospitaler og især i landbruget bruges meget antibiotika, og der skaber resistente bakterier i resten af samfundet.
To typer bakterier

Grampositive bakterier har en cellevæg, som yderst har en tyk cellevæg som består af peptidoglycan, som består af en kompleks opbygning disakkarider og korte peptidkæder. Inderst har den en cellemembran.
Gramnegative bakterier har en dobbeltmembran og en tyndere cellevæg i midten.
Før vi kan komme videre skal du lære at skelne mellem to typer bakterier. Gram positive og gram negative. Der flere billioner (1012) bakterier fordelt på flere tusinde slægter. Størrelsesforskellen på bakterier er større, end hvad vi finder hos landlevende dyr. Men der er to hovedtyper vi opdeler dem i efter deres cellevæg. Gram positive og gram negative, og deres opbygning har betydning for hvordan antibiotika rammer dem.
Video med gennemgang af figurerne på siden
Sådan rammer antibiotika bakterierne
forstyrrer dannelsen af cellevæggen ved at enzymet transpeptidase, som skal danne peptidbindinger blokeres. Desuden kan de aktivere bakteriens egne enzymer, som nedbryder cellevæggen. De rammer primært grampositive bakterier. Cellen brister pga. osmotisk overtryk.
Rammer også cellevæggen. Binder sig til cellevæggen i grampositive celler, og blokerer for korrekt opbygning af den, og desuden blokerer den for tværbindinger i cellevæggen. som skulle gøre den mere holdbar.
Rammer dannelse af cellevæggen ved at blokere for enzymet transpeptidase, så peptidoglucan ikke kan dannes. De aktiverer også enzymer i celler, som nedbryder cellevæggen.
Blokerer translationen i proteinsyntesen ved at binde sig til A-pladsen i ribosomet så tRNA ikke kan binde sig.
Bredspektret antibiotika som hæmmer proteinsyntesen ved at forhindre dannelsen af peptidbindinger, som skal til for at bygge et polypeptid.
Angriber proteinsyntesen ved at binde sig til ribosomerne. De kan både blokere for translationen, eller give et fejlagtigt polypeptid. De rammer hovedsageligt gram negative bakterier.
Forstyrrer produktion af DNA og dermed replikationen

Et eksempel på hvordan tetracyklin angriber ribosomets A-plads, så tRNA ikke kan binde sig og aflevere en aminosyre. Det stopper proteinsyntesen og bakterien vil dø.
Hvordan opstår resistens?
Antibiotika findes naturligt i naturen, og derfor findes forsvaret også i bakteriernes gener. I takt med vi skaber et miljø med mere antibiotika, dukker der flere resistente bakterier op.
Det er ikke fordi mutationer skaber flere resistente gener, men i en verden med meget antibiotika får de lov at teste og vinde kapløbet om overlevelse, Den fordel ville de ikke have uden udbredt brug af antibiotika.
Bakterier deler resistens med hinanden
Når to bakterier mødes, kan de udveksle DNA – også til andre bakteriestammer ved konjugation. Bakterier har både kromosomalt DNA og ofte plasmider, og det er i de sidste gener for resistens findes.
Bakterier kan også samle plasmid-DNA op ”fra gaden” og bruge det. Det kan være plasmider fra dræbte bakterier. Processen kaldes transformation.
En sidste måde resistente gener kan overføres til bakterier er ved hjælp af transduktion. Bakteriofager (virus som inficerer bakterier) angriber en bakterie ved at indsprøjte DNA (eller RNA) ind i cellen og bruge den til at danne kopier af sig selv. Nogle gange vil den bringe et stump DNA med fra en tidligere angrebet bakterie – og den kan indeholde resistens-DNA.

Bakterien til venstre har et plasmid med et resistensgen. Den bryder hydrogenbindingerne i DNA-strengen, og sender den ene halvdel igennem en pili, som er et rør de to bakterier har dannet mellem hinanden. I fjerde billede har hver bakterie hver deres komplementære streng af plasmidet, og de går i gang med at sætte de manglende komplementære nukleotider på, indtil de har et færdigt dobbeltstrenget plasmid.

Ved transformationen optager bakterien et plasmid med resistens fra omgivelserne.

Ved transduktionen angriber en bakteriofag bakterien ved at sprøjte sit DNA ind i cellen. Med sig har den et resistensgen, som er en rest fra et tidligere angreb på en anden bakterie.
Mutationer skaber resistens
Indtil nu har vi flyttet rundt på eksisterende resistensgener, men mutationer er eneste kilde til nye resistenser. De typiske mutationer, som skaber resistens, er punktmutationer.
Eksempler på mutationer
- Fx opstår resistens mod tuberkulosemedicin ved at ændre RNA-polymerase, så antibiotikummet ikke kan binde sig til det.
- Mutationer i proteinkanaler ændres, så antibiotika har sværere ved at transportere antibiotika ind i cellen.
- Mutation sætter turbo på den pumpe, som pumper uønskede stoffer, som fx antibiotika, ud af cellen.
- Ændring af enzymer, så de angriber mere bredt. De nedbryder ikke kun det sædvangelige substrat, men nu også antibiotika.
- Ændring i ribosomet, hvor fx erythromycin eller tetracyklin angriber, så det ikke længere kan binde og blokere proteinsyntesen. (se figur)
- Mindske antibiotikas evne til at binde til cellevæggen, så fx antibiotikummet sulfoamid ikke kan binde sig og blokere for dannelsen af cellevæggen.
Tre eksempler på modangreb mod antibiotika
Bakterier lader sig ikke slå ud, og de har flere modtræk mod antibiotika. Her er tre eksempler.

1. Mutation ændrer proteinkanal, så antibiotika har sværere ved at blive transporteret ind i cellen. 2. Enzymer ændres ved mutationer, så de også kan nedbryde antibiotika. 3. Genet for proteinpumpen rammes, så den pumper mere antibiotika ud af cellen.
Resistens er evolution vi kan observere
Da dine forældre var på din alder, var multiresistente bakterier sjældne, men det er de ikke i dag. Fremkomsten af flere og flere multiresistent bakterier er en livstrussel mod mange mennesker.
Hvis du har halsbetændelse, så overlever du nok at streptokokbakterierne er blevet resistente, men der er livstruende sygdomme med infektion af resistente bakterier, hvor læger står næsten uden mulighed for behandling. Vi kan bruge vores viden om evolution til at vende udviklingen.
Der er tre elementer som skal være til stede før der sker evolution.
- overflod af afkom. Bakterier kan dele sig på 20 minutter, og med en eksponentiel vækst kan de opnå enorme antal på kort tid.
- Mutationer er kilden til variation hos bakterier.
- naturlig selektion. I et miljø vil meget antibiotika giver vi de resistente bakterier en selektionsfordel. Dvs. vi give dem gunstige betingelser som gør at de formerer sig hurtigere end de ikke-resistente. Se fig.
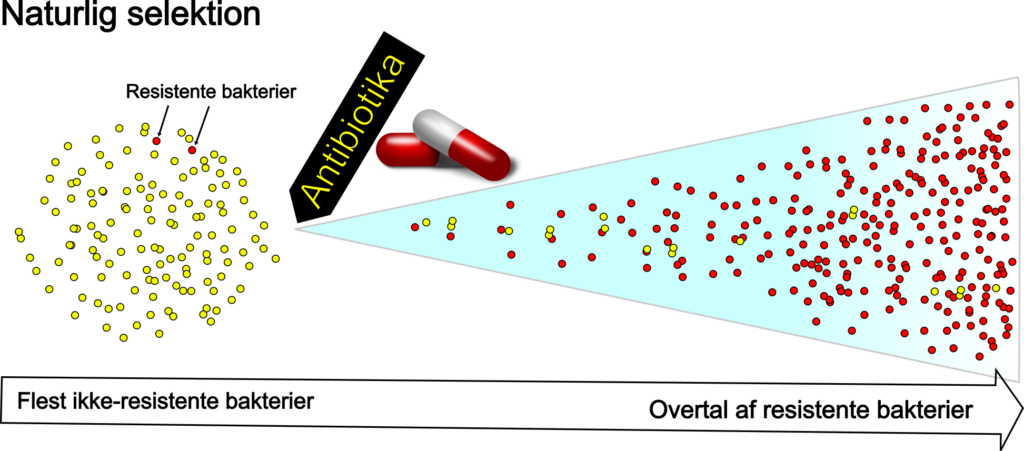
Løsning: Hvis vi ændrer miljøet, hvor resistente bakterier ikke længere har en konkurrencefordel (øget fitness), vil de gå kraftigt tilbage. Mange af mutationerne er ikke gratis for bakterierne, og de er faktisk svækket i forhold til de ikke-resistente bakterier, og derfor vil de blive slået i en konkurrence uden antibiotika i miljøet.
Derfor bør vi bruge så lidt antibiotika som muligt, og gemme den gavnlige virkning af vidundermedicinen til dem som er virkeligt syge. Det skal ske i alle lande, så de lande der bruger meget antibiotika ikke kommer til at fungere som laboratorier for udviklingen af nye resistenser til skade for befolkningen i hele verden.
